- · 《中学化学》栏目设置[06/30]
- · 《中学化学》数据库收录[06/30]
- · 《中学化学》收稿方向[06/30]
- · 《中学化学》投稿方式[06/30]
- · 《中学化学》征稿要求[06/30]
- · 《中学化学》刊物宗旨[06/30]
约克大学《化学·科学》自组装的低分子量胶凝剂
作者:网站采编关键词:
摘要:【科研摘要】 最近, 约克大学 David K. Smith 研究团队 报告了通过结合低分子量胶凝剂(LMWG)DBS-CONHNH2和天然多糖藻酸钙聚合物胶凝剂(PG)制备混合自组装微凝胶珠。 由于自组装网络的
【科研摘要】
最近,约克大学David K. Smith研究团队报告了通过结合低分子量胶凝剂(LMWG)DBS-CONHNH2和天然多糖藻酸钙聚合物胶凝剂(PG)制备混合自组装微凝胶珠。
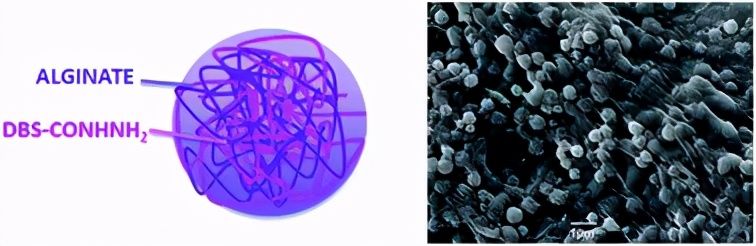
由于自组装网络的脆弱性和保持任何施加形状的困难,基于LMWG的微凝胶配方极为罕见。该杂化珠包含互穿的LMWG和PG网络,并且是通过乳液法获得的,可以制备直径在mm或μm范围内的大小可控制的球形凝胶颗粒。相关论文以题为Self-assembled low-molecular-weight gelator injectable microgel beads for delivery of bioactive agents发表在《Chemical Science》上。基于LMWG /藻酸盐的微凝胶可以很容易地制备,其可再现的直径<1μm(约800 nm)。它们在室温下在水中稳定数月,并能通过注射器注射。LMWG在冷却时的快速组装在帮助控制微凝胶珠的直径方面起着积极的作用。

这些LMWG微珠保留了母体凝胶传递生物活性分子肝素的能力,并且在细胞培养基中增强了人间充质干细胞的生长。因此,这种微凝胶在组织修复中可能具有未来的应用。这种制造LMWG微凝胶的方法是一种平台技术,可以潜在地应用于各种不同功能的LMWG,因此具有广泛的潜力。
【主图见析】
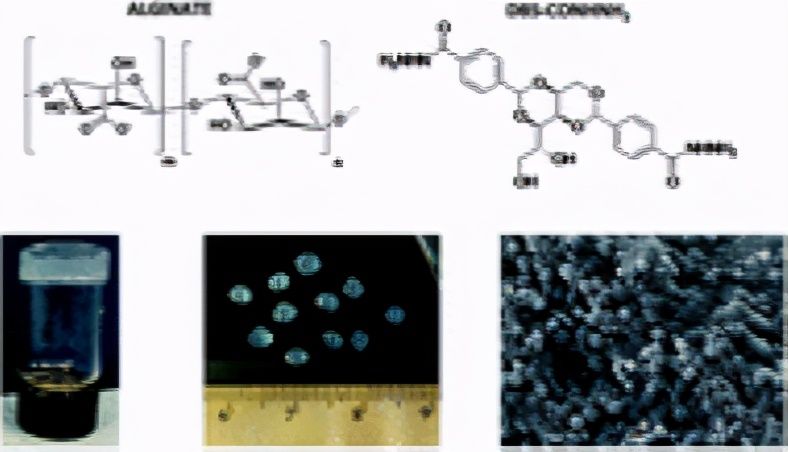
图1海藻酸钠和DBS-CONHNH2的化学结构,以及从左到右的通过乳液法制备的小瓶,毫米级微珠和微凝胶微珠中DBS-CONHNH2 /海藻酸钠凝胶的图像。
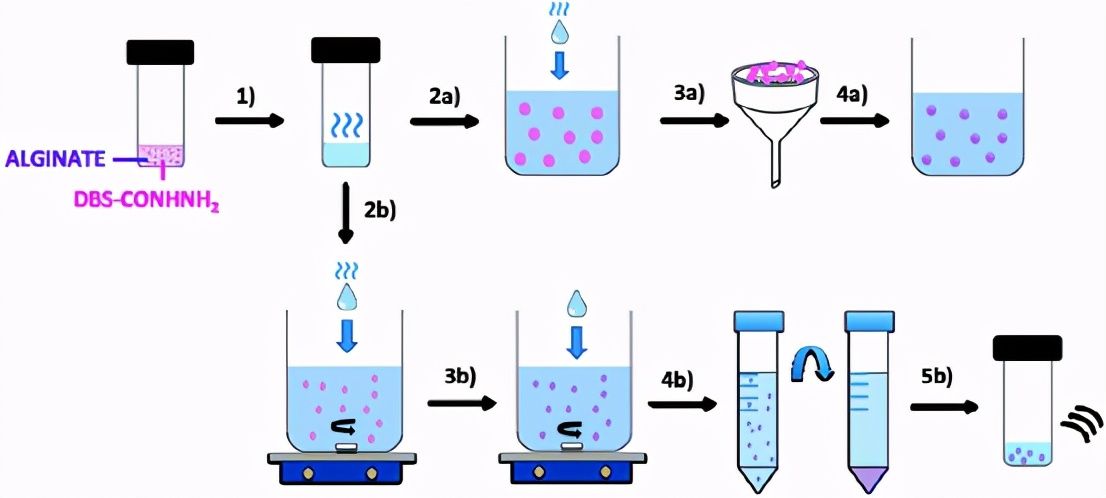
图2.乳液法制备DBS-CONHNH2/藻酸盐凝胶珠和微凝胶的示意图。加热DBS-CONHNH2(0.3%wt/vol)和藻酸盐(0.5%wt/vol)的混合物,直到LMWG完全溶解。为了获得杂化凝胶珠,将热溶液滴加到石蜡油(2a)中。然后通过过滤(3a)收集凝胶滴,并将其转移到CaCl 2溶液(5.0%wt / vol)中以使藻酸盐(4a)交联。或者,为了获得微凝胶,在搅拌下将DBS-CONHNH2/藻酸盐热溶液滴加到石蜡油和Span80的混合物中(2b)。1小时后,加入CaCl2(5.0%wt / vol),并将乳液再搅拌20分钟(3b)。然后将样品转移到猎鹰管中,并将微凝胶颗粒通过用石油醚,乙醇和水多次洗涤和离心循环进行纯化(4b)。最后,将样品转移到样品瓶中并进行超声处理,以帮助分散颗粒(5b)。
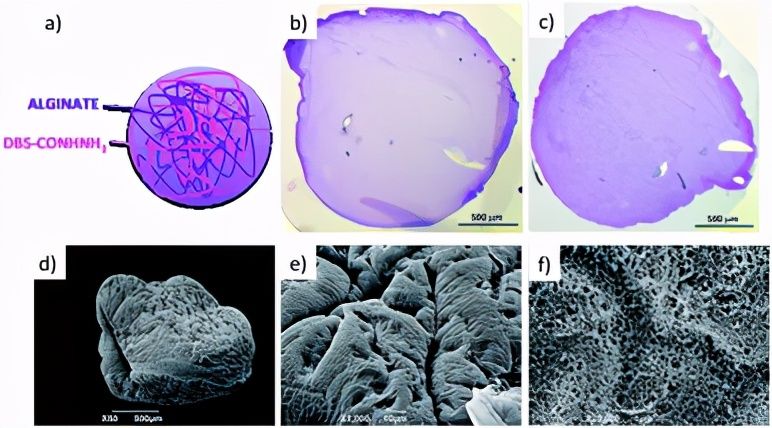
图3(a)是凝胶珠内两个胶凝剂的空间布置的示意图。(b和c)嵌入在树脂中并使用甲苯胺蓝(比例尺500μm)着色的凝胶珠的横截面的光学显微镜。(d)整个凝胶床的SEM,(e)凝胶珠表面和(f)横截面(比例尺为500、10和1μm)。

图4(a)DBS-CONHNH2 /藻酸盐双组分微凝胶和(b)藻酸盐微凝胶的SEM图。左边的图像是新准备的,右边的图像是30天后的图像。比例尺:1μm((a)左)和5μm((a)右,(b)左和右)。
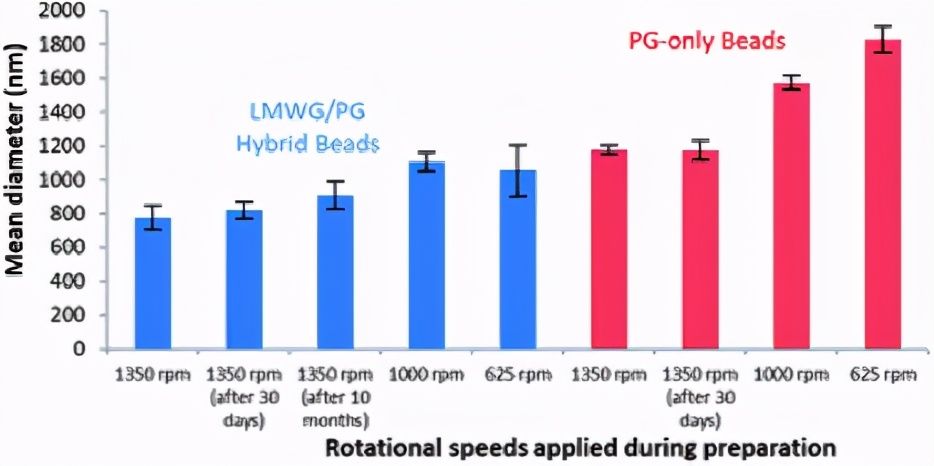
图5用不同的转速制备的DBS-CONHNH2/藻酸盐双组分微凝胶(蓝色)和仅藻酸盐微凝胶(红色)的DLS测量体积分布。
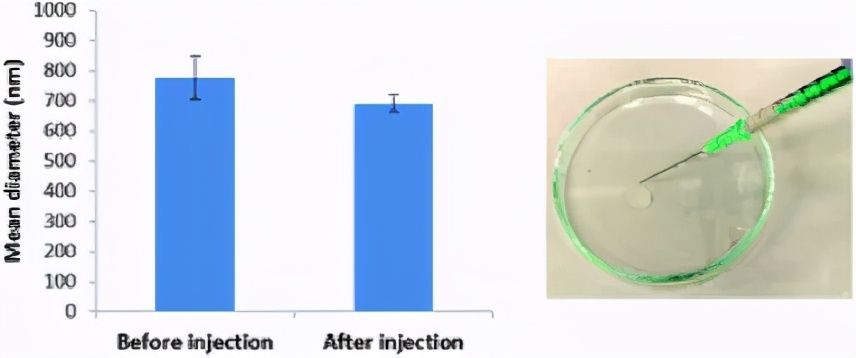
图6(左)通过注射器注射之前和之后,以1350 rpm的速度混合制备的DBS-CONHNH2/藻酸盐双组分微凝胶的平均直径。(右)通过注射器注射的DBS-CONHNH2/藻酸盐双组分微凝胶的照片。
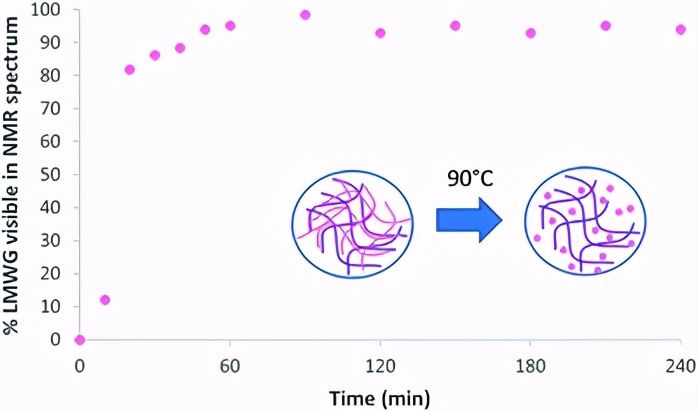
图7在NMR光谱仪中于90°C加热不同时间后,通过1H NMR可视化的DBS-CONHNH2的百分比,因此在液体状流动相中。示意图表示在LMWG/PG混合凝胶微珠中LMWG网络的热诱导分解。
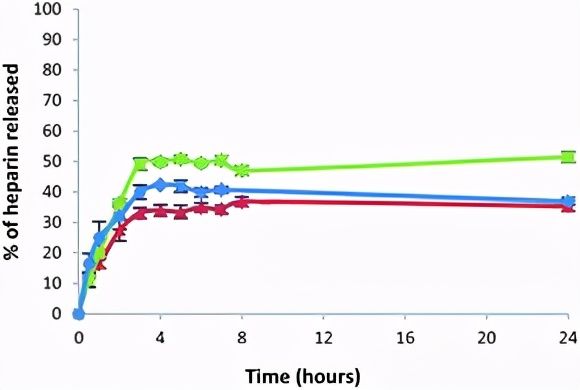
图8在10 mM Tris-HCl/150 mM NaCl缓冲液中随时间释放的肝素百分比:DBS-CONHNH2/藻酸盐多组分凝胶在小瓶中(红色三角形),凝胶珠(绿色正方形)和微凝胶珠(蓝色圆圈)。
文章来源:《中学化学》 网址: http://www.zxhxzz.cn/zonghexinwen/2021/0328/967.html